
乙二胺四乙酸簡稱EDTA或者EDTA酸,分子式為C10H16N2O8 ,用H4Y表示其結構式如圖1所示。
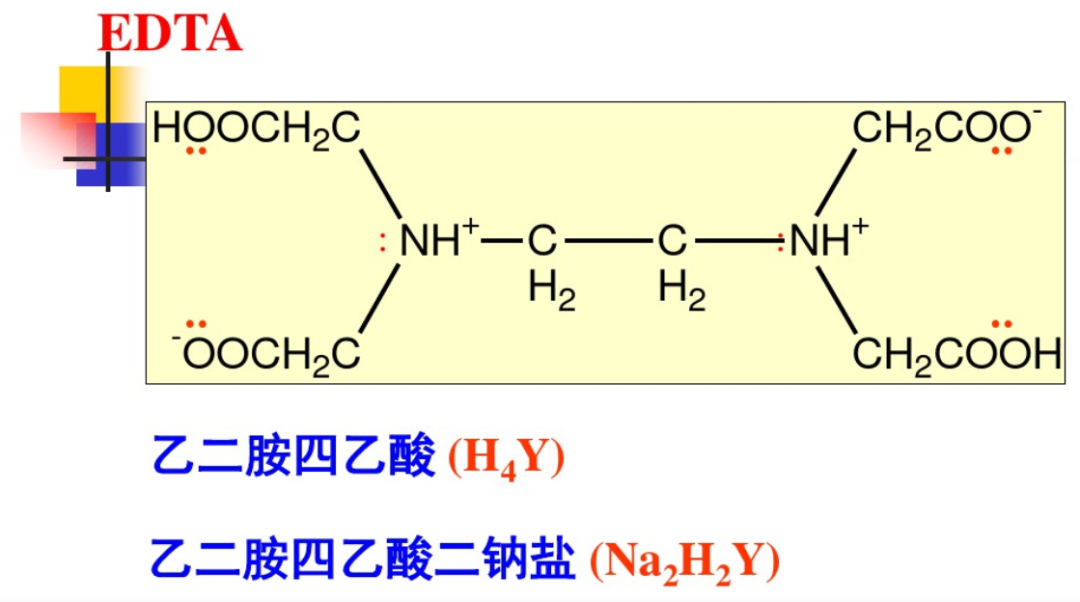
圖1:乙二胺四乙酸結構式
當H4Y溶于水時,不僅可以將自身的H+給出去,形成不同形式的HXY(4-x)-陰離子;當溶液酸度很高時,H4Y的兩個羧基可以接受H+分別以H5Y+或H6Y2+陽離子的形式存在于溶液中。因此EDTA在水溶液中可以H6Y2+、H5Y+、H4Y、H3Y-、H2Y2-、HY3-、Y4-等7種形式存在,而它們在水溶液中的具體存在形式及分布分數與溶液pH息息相關(如圖2所示)。
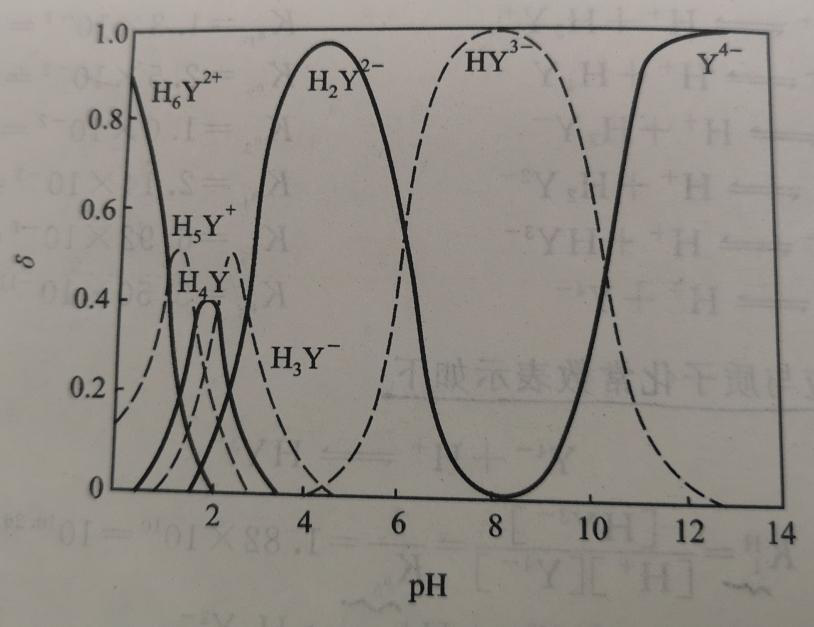
圖2:EDTA各種存在形式的分布圖
EDTA與金屬離子形成螯合物時,它的氮原子和氧原子與金屬離子鍵合形成具有多個五原子環的立體螯合物。EDTA螯合物的立體構型如圖3所示。一般情況下,這些絡合反應將按照1:1的比例進行反應。
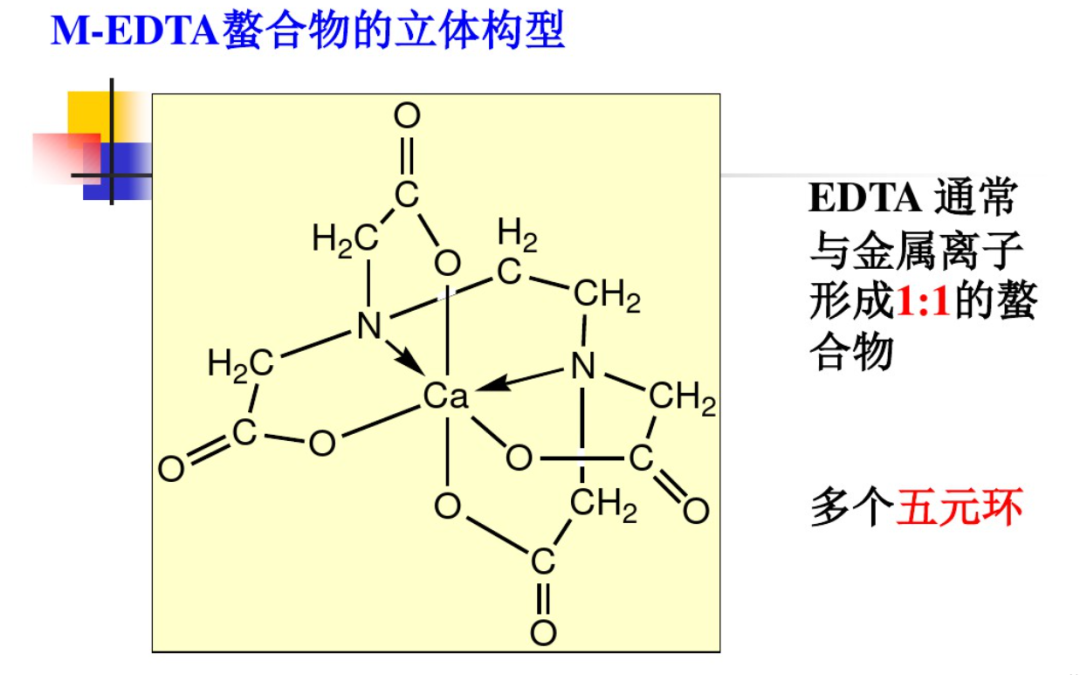
圖3:EDTA-M螯合的立體結構
例如在ZnCl2的滴定實驗中,以EDTA-2Na作為滴定劑,鉻黑T指示液作為指示劑,于氨-氯化銨緩沖溶液(pH=10)中滴定待測ZnCl2標準滴定溶液。當溶液滴定至由藍色變為紫紅色時,此時達到反應終點,以消耗EDTA-2Na的體積根據公式(1)計算ZnCl2標準滴定溶液的濃度(需要同時做空白試驗扣除空白的影響)。
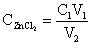
C1:EDTA-2Na標準溶液的濃度
V1:消耗EDTA-2Na的體積
V2:消耗ZnCl2標準滴定溶液的體積
EDTA由于其良好的化學性質,被廣泛應用于化學分析中。迄今為止,它已經成為分析化學中應用guang泛的螯合劑。EDTA除了作為螯合劑用于絡合滴定外,還作為掩蔽劑等應用于各種分離和測定方法中。
